في خلال فترة امتدت لأكثر من عامين التي توفرت في الولايات المتحدة لقاحات COVID «كوفيد - 19»، لم تتغير الوصفة الأساسية لمكافحته إلا قليلاً. وفي غضون ذلك، كشف الفيروس عن خمسة متغيرات اكتسب كل منها اسماً من أسماء الحروف اليونانية الخاصة بها، تلتها مجموعة من المتغيرات الفرعية المسماة «أوميكرون» ذات الألقاب الغريبة، ويبدو أن كلاً منها ينتشر بشكل أسرع من الأخير.
واللقاحات، التي تستغرق شهوراً لإعادة صياغتها، لا تستطيع مواكبة فيروس يبدو أنه يعيد اختراع نفسه خلال أسبوع.
تعثّر جهاز المناعة
الطفرة التطورية لفيروس «سارس - كوف - 2» المسمى «كوفيد - 19» قد لا تكون السبب الوحيد لحالات تعثر المناعة في مواجهتها لمتغيرات الفيروس. إذ يبدو أن الجسم يركز على النسخة الأولى من الفيروس الذي واجهه، إما عن طريق الإصابة بالعدوى أو بعد تلقي حقن اللقاح الأول.
وهذا الانشغال بالماضي - الذي يمارسه جهاز المناعة - هو الذي يسميه الباحثون «الخطيئة الأصلية للمستضد»، قد يترك الإنسان مع دفاعات غير مصممة بشكل جيد لمواجهة متغيرات الفيروس اللاحقة. (الخطيئة الأصلية للمستضد) «original antigenic sin» تظهر عندما يحتفظ الجسم بذاكرة مناعية خاصة ضد العدوى الأولى. وتتجسد الذاكرة في النشاطات المضادة من قبل الخلايا المناعية - المحرر).
في الأشهر الأخيرة، بدأ بعض الخبراء في إبداء القلق من أن هذه «الخطيئة» قد تقوض الآن اللقاحات المحدّثة. لذا يذهب تفكير بعضهم إلى أقصى حد، مشيرين إلى أن الناس قد لا يحصلون على الكثير من الحماية من حقن لقاحات «كوفيد» الجديدة، التي لا تتطابق مع أول نسخة من الفيروس.
وتشير البيانات الأخيرة إلى هذا الاحتمال. ويبدو أن الإصابات السابقة بالفيروس، أو تلقي اللقاح الأصلي الأول، تعمل على تشكيل أو حتى إخفاء ردود أفعال الناس تجاه اللقاحات الجديدة ثنائية التكافؤ. أخبرتني جينا جوثميلر، عالمة المناعة في كلية الطب بجامعة كولورادو: «ليس لدي شك في ذلك... إذ لا يصنع الجهاز المناعي الآن الأجسام المضادة المركزة على (أوميكرون) بالكمية أو الجودة المطلوبة مثلاً لو كان الجهاز قد صادف (أوميكرون) لأول مرة».
لكنْ هناك أيضاً جانب إيجابي لهذا العناد الذي لا يمكننا العيش من دونه، كما تقول كاتلين جوستيك، عالمة المناعة ومصممة نماذج الأمراض المعدية التي درست ظاهرة الإنفلونزاـ فـ«الخطيئة الأصلية للمستضد» هي السبب في تكرار العدوى، التي تصبح في المتوسط أكثر اعتدالاً بمرور الوقت. وأضافت جوستيك: «إنه جزء أساسي من القدرة على تكوين ذاكرة مناعية».
وهكذا، فإن الانطباعات الأولى القوية عن هذا الفيروس التاجي يمكن ويجب أن تؤثر على كيف ومتى وكم مرة نعيد التطعيم ضده. ويمكن أن يساعد الفهم الأفضل لدرجة استمرار هذه الانطباعات العلماء أيضاً في معرفة سبب مقاومة (أو عدم مقاومة) الأشخاص الذين يكافحون أحدث متغيرات الفيروس - وكيف ستعمل دفاعاتهم ضد الفيروس مع استمرار تغيره.
خطيئة العدوى الأولى
ان أسوأ شيء في «الخطيئة الأصلية للمستضد» هو اسمها. ويقع اللوم في ذلك من الناحية الفنية على توماس فرانسيس جونيور، عالم المناعة الذي صاغ العبارة منذ أكثر من ستة عقود بعد أن لاحظ أن عدوى الإنفلونزا الأولية التي تعرض لها الأشخاص في مرحلة الطفولة يمكن أن تدفع الجسم لأن يتحيز في تعامله مع السلالات اللاحقة.
يقول جابرييل فيكتورا، عالم المناعة في جامعة روكفلر: «في الأساس، إن الإنفلونزا التي تصاب بها أولاً في الحياة هي التي تستجيب لها بشدة على المدى الطويل». يمكن أن يصبح ذلك مشكلة إلى حد ما عندما تأتي سلالة مختلفة المظهر تماماً. في مثل هذه السيناريوهات، قد تبدو الخطيئة الأصلية للمستضد شبيهة إلى حد كبير بالحالة البيولوجية لمراهق متحمس يتألم بسبب انهيار علاقة طيبة سابقة، أو لطالب «لم يتخرج أبداً في المدرسة الابتدائية المناعية».
ولكن من وجهة نظر الجهاز المناعي، فإن عدم نسيان الأمر الأول هو أمر منطقي. ولذا فإن المواجهات الجديدة مع أحد العوامل الممرضة تؤدي إلى مباغتة الجسم على حين غرة - وتميل إلى أن تكون الأشد في تأثيراتها.
إن رد الفعل الدفاعي عميق الجذور. إذن فهو أمر عملي، فهو يزيد من فرص مقاومة العدوى الغازية نفسها في المرة القادمة، إذ سيتم تحديدها ومجابهتها بسرعة.
وقال فيكتورا: «إن امتلاك ذاكرة جيدة والقدرة على تعزيزها بسرعة كبيرة أمر جيد جداً في بعض الأحيان. إنها طريقة الجسم للتأكد من أنه لن ينخدع مرتين».
تأتي هذه الخصائص القديمة بمزايا واضحة حتى عندما تتحول الميكروبات إلى أشكال جديدة، كما تفعل فيروسات الإنفلونزا وفيروسات كورونا في كثير من الأحيان. وبما أن المسببات الممرِضة لا تعيد تكوين نفسها دفعة واحدة، لذا فإن الخلايا المناعية التي تستوطنها مقتطفات مألوفة من الفيروس يمكنها في كثير من الحالات القضاء على عدد كافٍ من الغزاة الجدد لمنع أسوأ آثار العدوى.
ولهذا السبب فحتى لقاحات الإنفلونزا التي لا تتوافق تماماً مع سلالات الموسم الأكثر بروزاً لا تزال جيدة جداً في تقليل الدخول إلى المستشفيات، أو الوفيات. وقالت جوثميلر: «هناك الكثير من التأخير في مدى تغير الفيروس قبل أن نفقد الحماية حقاً... إن مساحة المناورة يجب أن تكون أكبر مع SARS - CoV - 2. لأن متغيراته الفرعية تميل إلى أن تكون أكثر تشابهاً مع بعضها البعض، مقارنة بسلالات الإنفلونزا المختلفة، على سبيل المثال.
مع كل الإيجابيات التي يمكن أن تقدمها الذاكرة المناعية، يميل العديد من علماء المناعة إلى توجيه أعينهم إلى الآثار الأخلاقية السلبية والغريبة لعبارة «الخطيئة الأصلية للمستضد». يقول ديبتا بهاتاشاريا، عالم المناعة في جامعة أريزونا: «أنا حقاً، أكره هذا المصطلح». بدلاً من ذلك، فهو يفضل مع آخرين استخدام كلمات أكثر حيادية مثل «الانطباعة»، كما حال انطباعة البطة الحديثة الولادة التي تلتصق بأول شخصية من الأمهات. يقول رافي أحمد، اختصاصي المناعة في جامعة إيموري: «هذه ليست ظاهرة مناعية غريبة». إنه مثال كتابي لما يفعله نظام مناعي قابل للتكيف وعالي الأداء، ويمكن أن يكون له آثار إيجابية أو سلبية، اعتماداً على السياق.
أظهرت حالات تفشي الإنفلونزا الأخيرة القليل من كل من الآثار: خلال جائحة H1N1 عام 2009. كان أداء العديد من كبار السن، الذين عادة ما يكونون أكثر عرضة لفيروسات الإنفلونزا، أفضل مما كان متوقعاً ضد السلالة المتأخرة، لأنهم قد تعرضوا لحالة مشابهة ففيروس H1N1 - مشتق من الإنفلونزا الإسبانية في جائحة 1918 - في شبابهم. ولكن في بعض المواسم التي تلت ذلك، تسبب فيروس H1N1 في إصابة البالغين في منتصف العمر بشكل غير متناسب، لأن عدم إصابتهم بالإنفلونزا في بداية حياتهم أدى ذلك إلى إبعادهم عن الاستجابة الوقائية.
جزء من ردود الفعل تلك يعود إلى الحركية المطلقة: تميل الخلايا المناعية المخضرمة، المدربة على المتغيرات والسلالات السابقة، إلى أن تكون أسرع في الاستجابة من الخلايا المناعية الجديدة، كما يقول سكوت هينسلي، عالم المناعة في كلية بيرلمان للطب بجامعة بنسلفانيا. وكلما زاد عدد الخلايا المتمرسة، زادت احتمالية قيامها بمزاحمة الخلايا المناعية المبتدئة - مما يحرمها من تجربة ساحة المعركة. وإذا عادت السلالة الفيروسية الأحدث في النهاية لتكرار العدوى، فإن تلك الخلايا المناعية الأقل خبرة قد لا تكون مستعدة بشكل كافٍ - مما يجعل الناس أكثر ضعفاً، ربما، مما قد يكونون لولا ذلك.
* ذي أتلانتيك
ـ خدمات «تريبيون ميديا»
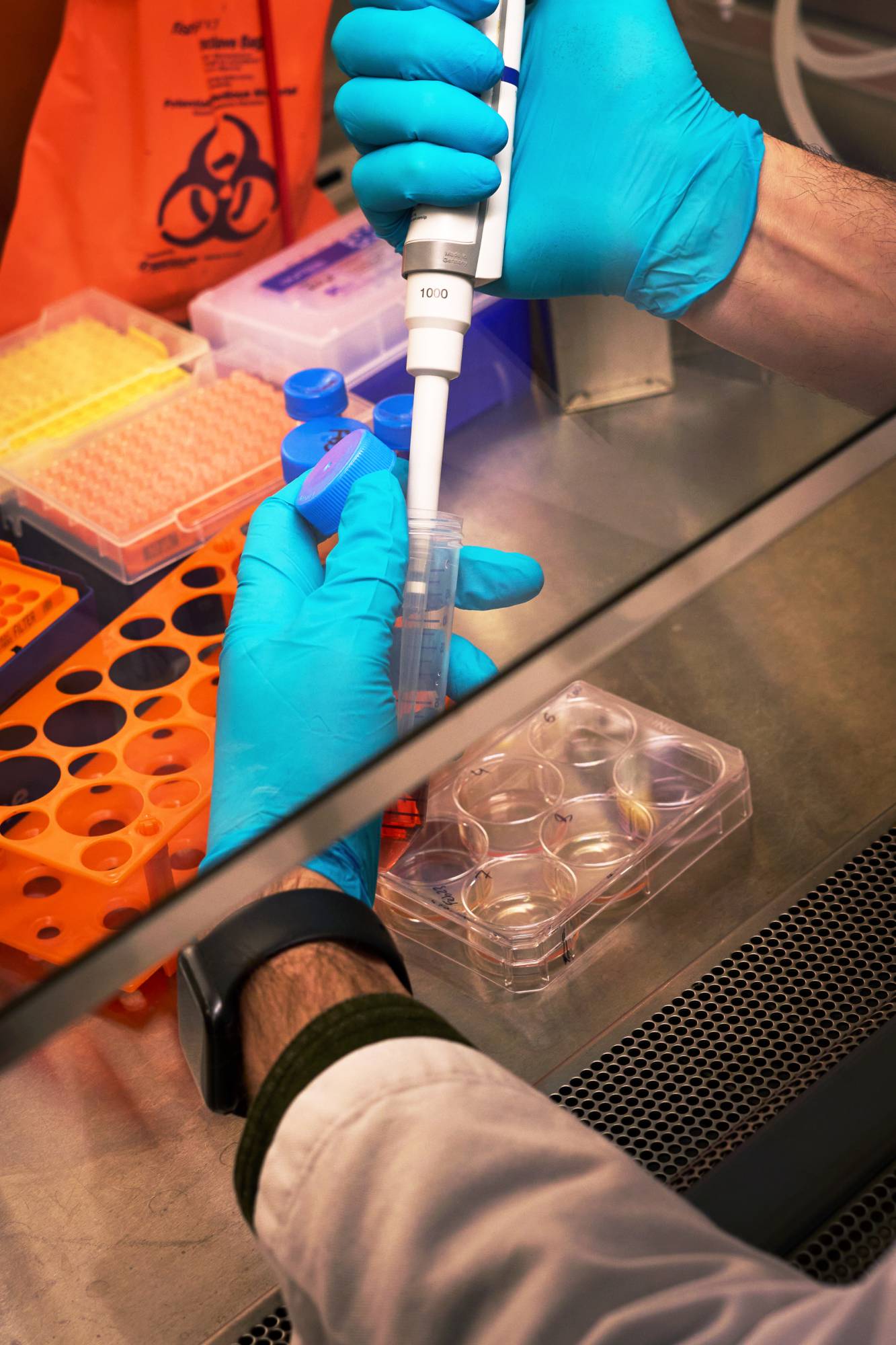
جسم الإنسان يتكيف بصعوبة لمقاومة متغيرات «كورونا»
أجهزتنا المناعية متعثرة ولا تزال عالقة في 2020


جسم الإنسان يتكيف بصعوبة لمقاومة متغيرات «كورونا»

لم تشترك بعد
انشئ حساباً خاصاً بك لتحصل على أخبار مخصصة لك ولتتمتع بخاصية حفظ المقالات وتتلقى نشراتنا البريدية المتنوعة