توجد أمام الباحثة إستر أولواغبينغا، بيضةٌ على حامل ثلاثي أزرق، وقد قُطعت نافذة مثلثة صغيرة في قشرتها. وعندما وضعت أولواغبينغا الفتحة تحت المجهر، كشفت عن جنين الدجاجة في الداخل.
أجنة الدجاج المختبرية
في يومه الثالث، تطوّر الجنين إلى سحابة ضبابية، بقلب نابض بحجم رأس الدبوس.
وتتدفق الخلايا عبر شرايين قرمزية اللون بشكل متقطع، كحركة المرور في ساعة الذروة.
إستر أولواغبينغا Esther Oluwagbenga، عالمة في شركة ناشئة للتكنولوجيا الحيوية تُدعى «نيون بايو» (Neion Bio)، وهي واحدة من العلماء القلائل في العالم الذين يمتلكون مهارة الحقن في شريان جنين الدجاجة. تقول أولواغبينغا: «عندما رأيت أحدهم يفعل ذلك لأول مرة، اندهشت. أردت حقاً أن أتعلم كيف أفعل ذلك. لكن الأمر كان أكثر تعقيداً مما كنت أتصور. أتدرب (على ذلك) مرتين على الأقل أسبوعياً».
حقنة في شريان الجنين
لإثبات هذه العملية الاستثنائية، تأخذ أنبوباً بلاستيكياً طويلاً من خطاف رف وتضع أحد طرفيه في فمها. أما الطرف الآخر، فيحتوي على إبرة محملة بصبغة زرقاء.
وبينما تنظر الباحثة إلى الجنين على شاشة الكمبيوتر، تُدخل الإبرة عبر نافذة قشرة البيضة، إلى داخل الجنين، ثم إلى شريان. وبنفخة خفيفة، تدفع الصبغة إلى الوعاء الدموي. وما أن ينبض لب الكتكوت، حتى يتحول جهازه الدوري لوحةً زرقاء.

بيض الدجاج مصانع للأدوية
تُوظّف أولواغبينغا هذه المهارة الجديدة في مهمة شركة «نيون بايو»، وهي: تحويل بيض الدجاج مصانعَ للأدوية. فهي وزملاؤها يُجرون هندسة وراثية على الطيور لإنتاج مركبات طبية.
محاولات علمية دؤوبة
حاول العلماء على مدى ثلاثة عقود إنتاج الأدوية في البيض، ولكن النتائج كانت ضئيلة حتى الآن. ولم تُجز إدارة الغذاء والدواء الأميركية سوى دواء واحد مُنتَج من الدجاج للاستخدام في الولايات المتحدة، هو دواء «كانوما» Kanuma لعلاج اضطراب كبدي نادر، حصل على الموافقة في عام 2016، بتكلفة سنوية للمريض الواحد تبلغ 310000 دولار.
3 مركبات طبية
ولكن منذ ذلك الحين، سهّلت سلسلة من الاكتشافات عملية هندسة الدجاج. يقول كين-إيتشي نيشيجيما، عالم الأحياء بجامعة ناغويا في اليابان: «لقد تحسّن الوضع بشكل كبير».
وخرجت شركة «نيون بايو»، التي تأسست عام 2024، من مرحلة التأسيس السري يوم الخميس لتعلن عن اتفاقية لتطوير ثلاثة مركبات مع شركة أدوية كبرى. ولم تُحدّد الشركة في إعلانها الأدوية التي ستعمل عليها.
تكلفة علاج متدنية
وقال سام ليفين، أحد مؤسسي الشركة، إن استخدام البيض في صناعة الأدوية قد يُخفّض تكلفتها إلى عُشر أو حتى جزء من مائة من تكلفتها الحالية.
وأضاف: «إنها سلسلة إمداد طبي تعتمد على الحبوب الزراعية والماء».
حيوانات لإنتاج الأدوية
أما العديد من الأدوية الأكثر مبيعاً في العالم، مثل دواء السرطان كيترودا ودواء التهاب المفاصل هيوميرا، فهي عبارة عن بروتينات كبيرة ومعقدة، ولا يستطيع العلماء تصنيعها بالتفاعلات الكيميائية؛ لذا يقومون بهندسة خلايا من مبيض الهامستر الصيني لإنتاج هذه الأدوية.
الهامستر الصيني
كان اختيار مبيض الهامستر الصيني محض صدفة تاريخية. ففي أوائل القرن العشرين، رغب علماء في جامعات بكين في الحصول على حيوانات للدراسة. ولعدم تمكنهم من الحصول على فئران المختبر من الغرب، قاموا باصطياد الهامستر من الحقول المحيطة بالمدينة.
وفي نهاية المطاف، أثبت الهامستر فائدته الكبيرة لدرجة أن العلماء الأميركيين تمكنوا من الحصول عليه. وفي خمسينات القرن الماضي، اكتشف عالم الوراثة ثيودور باك أن خلايا مبيضه تقوم بأمر نادر الحدوث بين خلايا الثدييات (اللبائن): سهولة إنمائها مختبرياً.
واستخدم العلماء خلايا المبيض لدراسة الحمض النووي، وفي ثمانينات القرن الماضي، اكتشفوا كيفية هندستها بإضافة جينات أخرى، ثم استخلاص البروتينات المُصنّعة من تلك الجينات.
واليوم، تُزرع خلايا الهامستر الصيني في خزانات فولاذية ضخمة، لإنتاج دواء كيترودا والعديد من الأدوية الأخرى. لكن إنتاج الأدوية من هذه الخلايا ليس بالأمر الهين.
للحفاظ على نمو الخلايا في خزاناتها؛ يتعين على الفنيين إضافة مزيج معقد من المكونات والتخلص من النفايات الناتجة. قد تصل تكلفة تصنيع غرام واحد من الدواء إلى مئات أو آلاف الدولارات. وحتى المرافق اللازمة لزراعة الخلايا باهظة الثمن. في العام الماضي، بدأت شركة «ميرك» في بناء مصنع في ولاية ديلاوير لإنتاج دواء «كيترودا»، وستنفق الشركة مليار دولار على بنائه.
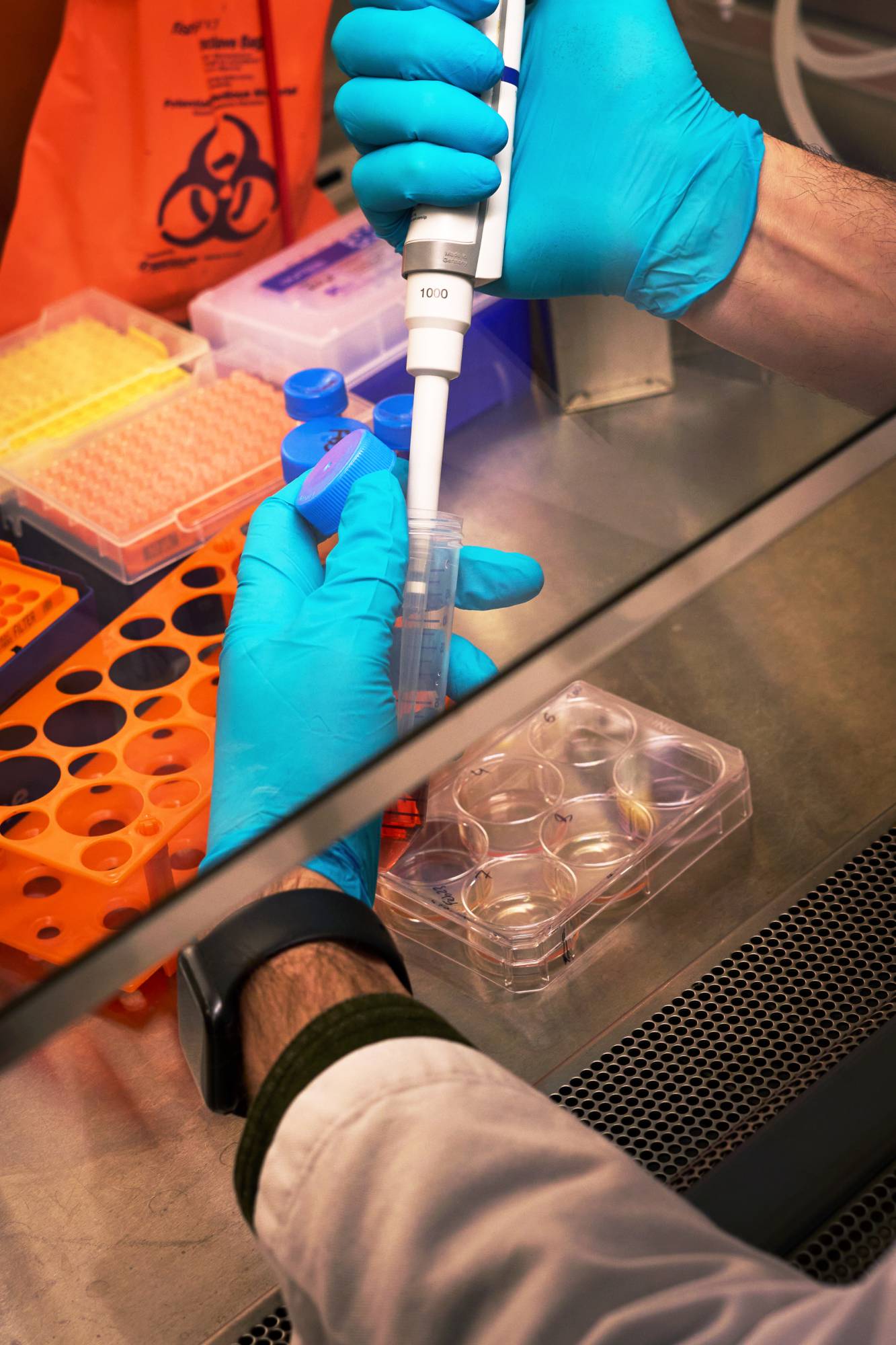
التوجه إلى بيض الدجاج
في تسعينات القرن الماضي، تساءل بعض العلماء عما إذا كان بيض الدجاج قد يوفر طريقة أفضل لإنتاج بعض هذه الأدوية. على عكس خلايا مبيض الهامستر الصيني، يُعدّ بيض الدجاج مصدراً غنياً بالبروتين؛ إذ يحتوي بياض البيضة الواحدة على 6 غرامات من البروتين. يقول جاي يونغ هان، عالم الأحياء في جامعة سيول الوطنية: «يمكن للبيض أن يعمل كمفاعلات حيوية مكتفية ذاتياً».
لكن تحويل البيض مصانعَ للأدوية لم يكن بالأمر السهل؛ إذ كانت التقنية معقدة للغاية.
وقال مايكل ماكغرو، عالم الأحياء في معهد روزلين بإدنبره، اسكوتلندا، والعضو في المجلس الاستشاري لشركة «نيون بايو»: «كانت التقنية بالغة الصعوبة». في معظم الأحيان، فشلت هذه التقنية في هندسة الحمض النووي للدجاج بشكل صحيح؛ ما أدى إلى سنوات من التجربة والخطأ لإنتاج طيور قادرة على إنتاج دواء بكفاءة.
وأسهم ماكغرو في تطوير أساليب أفضل. فقد استغل حقيقة أن الخلايا الجذعية للحيوانات المنوية والبويضات تدور في مجرى الدم في المراحل المبكرة من نمو جنين الطائر، ولا تهاجر إلى أعضائه التناسلية إلا لاحقاً. وقد ابتكر ماكغرو طرقاً لاستخلاص هذه الخلايا الجرثومية الأولية من أجنة الدجاج، ثم تنميتها بالملايين.
دجاج معدل وراثياً
سمح هذا التقدم للعلماء بإجراء تعديلات دقيقة على الحمض النووي للخلايا الجرثومية الأولية. في السنوات الأخيرة، أسس عدد من العلماء شركات للاستفادة من هذه التقنيات الجديدة، من بينها شركة «أفينوجين»، التي أسسها هان، وشركة «نيون بايو».
أخيراً... فقست الكتاكيت الأولى
لإنتاج أول قطيع من الدجاج المعدل وراثياً، أدخل فريق «نيون بايو»، جينات في الخلايا الجرثومية الأولية لإنتاج دواء في بياض البيض. وحقنت أولواغبينغا وزملاؤها الخلايا المعدلة في مجرى دم أجنة الدجاج. ثم أغلقوا قشرة البيض بإحكام وانتظروا حتى تنقر الكتاكيت طريقها للخروج.
فقست الكتاكيت الأولى في سبتمبر (أيلول) الماضي. والآن، يمتلك فريق «نيون» قطيعاً من 50 ديكاً من سلالة ليغورن المعدلة وراثياً.
* خدمة «نيويورك تايمز»