أصبح من الشائع أن نقرأ عن ظهور المواد البلاستيكية الدقيقة -القطع الصغيرة من البلاستيك بحجم صغير جداً- في كل مكان وفي كل شيء، بما في ذلك المحيطات، والأراضي الزراعية، والغذاء، والجسم البشري.
دقائق بلاستيكية نانوية
الآن، بدأ مصطلح جديد في الاستحواذ على الاهتمام: المواد البلاستيكية النانوية، وهي جسيمات أصغر حجماً من الدقائق الأخرى البلاستيكية الدقيقة، إذ إنها متناهية الصغر لدرجة تجعلها غير مرئية للعين المجردة (النانو واحد من المليار من المتر).
وبينما يكون حجم المواد البلاستيكية الدقيقة عادةً أقل عن 5 ملم، يتراوح عرض المواد البلاستيكية النانوية بين 1 و1000 نانومتر. وجدير بالذكر أن متوسط عرض شعرة الإنسان نحو ما بين 80000 و100000 نانومتر.
الملاحَظ أن المواد البلاستيكية النانوية تجتذب، اليوم، اهتماماً متنامياً بفضل التطورات التكنولوجية الحديثة، التي زادت قدرة الباحثين على اكتشافها وتحليلها.
وبفضل حجمها الأصغر، فإنها قادرة على التنقل بسهولة أكبر عبر مسافات طويلة، وإلى داخل بيئات أكثر تنوعاً عن المواد البلاستيكية الدقيقة. كما يمكنها اختراق الخلايا والأنسجة في الكائنات الحية بسهولة أكبر، ما قد يسفر عن تأثيرات سُمية مختلفة وأكثر حدة.
بلاستيك داخل الجسم البشري
وخلصت دراسات أُجريت عبر العامين الماضيين، إلى وجود مواد بلاستيكية نانوية في دم الإنسان، وكذلك في خلايا الكبد والرئة، وفي الأنسجة التناسلية مثل المشيمة والخصيتين. وعبر مختلف أنحاء العالم، عُثر على مواد بلاستيكية نانوية في الهواء ومياه البحر والثلج والتربة.
واليوم، ندرك بالفعل أن المواد البلاستيكية الدقيقة موجودة من مرتفعات جبل إيفرست إلى خنادق المحيط العميقة. وثمة أدلة كثيرة، حالياً، توحي بأن المواد البلاستيكية النانوية أوسع انتشاراً من المواد البلاستيكية الدقيقة الأكبر حجماً في البيئة.
«طرقات البلاستيك»
من أين تأتي وإلى أين تذهب؟ تنشأ المواد البلاستيكية النانوية عندما تتحلل منتجات الاستعمال اليومي، مثل الملابس، وأغلفة المواد الغذائية والمشروبات، والمفروشات المنزلية، والأكياس البلاستيكية، والألعاب، وأدوات النظافة. ويمكن أن يحدث هذا بسبب عوامل بيئية، مثل ضوء الشمس، أو التآكل الناتج عن عمل ميكانيكي. ويمكن لكثير من منتجات العناية الشخصية، مثل مستحضرات تقشير البشرة والشامبو، أن تطلق هي الأخرى مواد بلاستيكية نانوية.
ومثلما الحال مع الجزيئات البلاستيكية الأكبر، يمكن أن تأتي المواد البلاستيكية النانوية من مجموعة متنوعة من أنواع البوليمرات، بما في ذلك البولي إيثيلين والبولي بروبيلين والبوليسترين والبولي فينيل كلوريد. ونظراً لاستخدامنا المنتجات البلاستيكية على نطاق واسع، من الصعب تجنب وجود المواد البلاستيكية النانوية في حياتنا اليومية.
وعندما يصل البلاستيك إلى مقياس النانو، فإنه يطرح تساؤلات وتحديات فريدة، بسبب ضآلة حجمه الشديدة، وخصائص سطحه وتكوينه المتنوعة. ونظراً لصغر حجم البلاستيك النانوي، فإن بمقدوره بسهولة اختراق الخلايا والأنسجة التي يتعذر على الجزيئات الأكبر حجماً اختراقها. وإذا تراكمت المواد البلاستيكية النانوية داخل الكائنات الحية، فمن المحتمل أن تلحق بها أضراراً بيولوجية.
أما فيما يخص مصير المواد البلاستيكية النانوية في البيئة، فلا تزال تخضع لبحث مستمر. ولا يعرف العلماء على وجه اليقين، حتى الآن، ما إذا كانت المواد البلاستيكية النانوية تتحلل بشكل أكبر داخل بيئات مختلفة إلى جزيئات أصغر، أو إلى بوليمرات، وهي عبارة عن جزيئات كبيرة مكونة من الكثير من الجزيئات الصغيرة المرتبط بعضها ببعض.
رصد المواد البلاستيكية النانوية
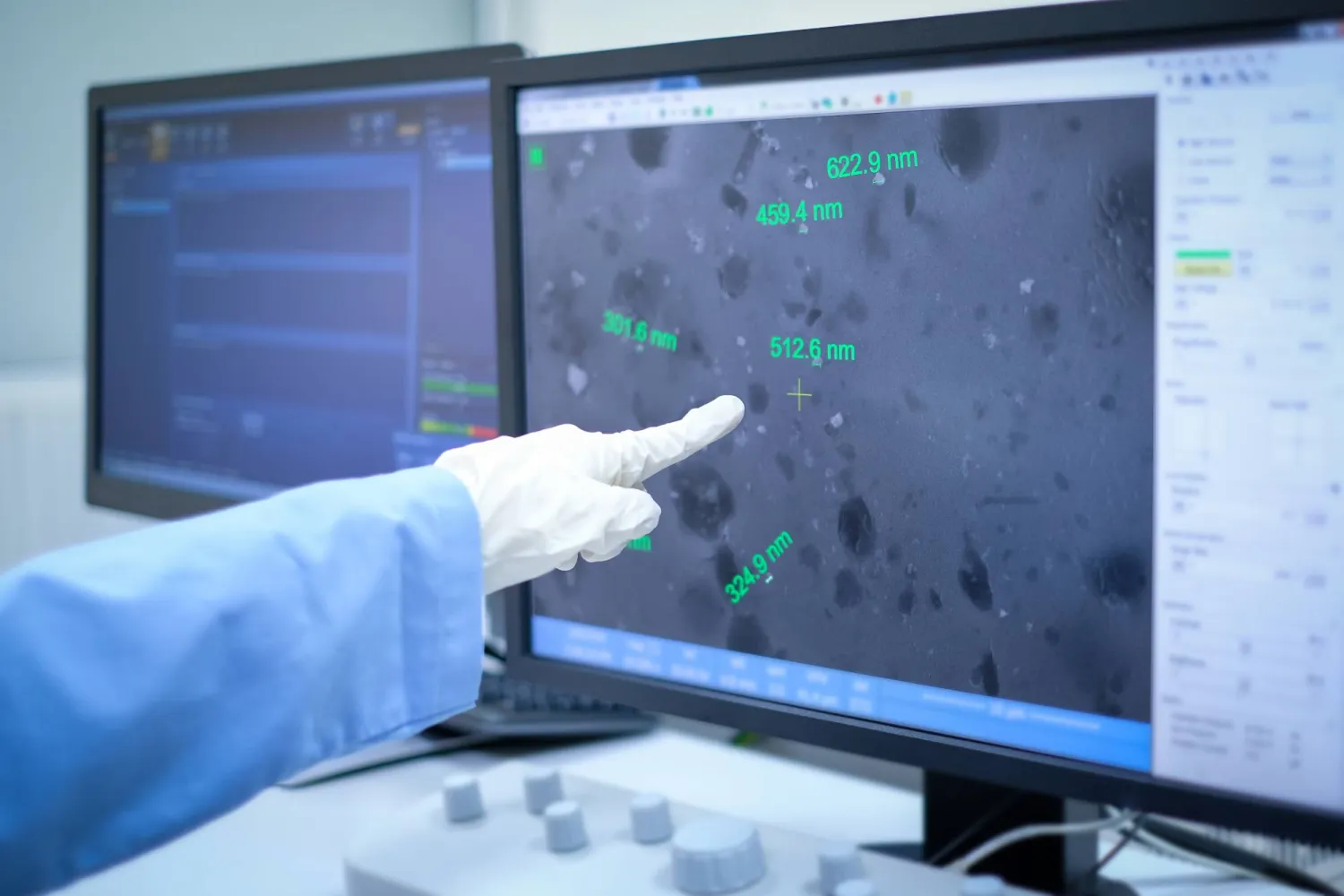
من الصعب العثور على المواد البلاستيكية النانوية، بسبب حجمها شديد الصغر، وتركيباتها وهياكلها الكيميائية المتنوعة. ويعكف الباحثون على تحسين طرق مختلفة للكشف عن المواد البلاستيكية النانوية، باستخدام تقنيات تتضمن تحليل «رامان» الطيفي Raman spectroscopy، والكروماتوغرافيا، وقياس الطيف الكتلي. ويمكن لهذه الطرق رصد الأشكال، وتحليل خصائص جزيئات البلاستيك النانوي.
وفي دراسة أُجريت عام 2024، طرح باحثون من جامعة كولومبيا تكنولوجيا جديدة تمكنت من رصد وحساب المواد البلاستيكية النانوية في المياه المعبأة، بحساسية ودقة عالية. وعلى عكس الدراسات السابقة التي لم تتمكن إلا من رصد كمية محدودة فقط من جزيئات البلاستيك النانوي، وجدت هذه الدراسة أن كل لتر من المياه المعبأة التي جرى تحليلها يحتوي على أكثر عن 010000 من الدقائق البلاستيكية، معظمها من البلاستيك النانوي.
ومن الضروري إجراء مزيد من الدراسات قبل أن يتمكن العلماء من حسم مسألة ما إذا كانت جميع المياه المعبأة تحتوي على مواد بلاستيكية نانوية. إلا أن هذه تكنولوجيا الرصد الجديدة تفتح الباب أمام مزيد من البحث.
دقائق بلاستيكية سامة
هل دقائق البلاستيك النانوية سامة؟ تشكل سُمية المواد البلاستيكية النانوية مجالاً آخر لا يزال البحث جارياً فيه.
يشير بعض الدراسات إلى أن هذه الجسيمات يمكن أن تحمل مخاطر كبيرة على النظم البيئية وصحة الإنسان. وخلصت إحدى الدراسات الحديثة إلى أنها قد تكون عامل خطر للإصابة بأمراض القلب. يتمثل مصدر قلق آخر في أن الملوثات الكيميائية والمعادن الثقيلة ومسببات الأمراض، قد تلتصق بالبلاستيكات النانوية، وتتركز في البيئة. ويمكن لهذه العملية أن تعرّض الكائنات الحية لتركيزات عالية من هذه المواد الضارة.
الواضح أن المواد البلاستيكية النانوية أصبحت جزءاً من البيئات الحديثة، لكنَّ العلماء بحاجة إلى مزيد من البحث والمعلومات، لفهم أنواع التهديدات التي يمكن أن تشكلها. وكما يقول علماء السموم في كثير من الأحيان: «الجرعة تصنع السم». وبعبارة أخرى، فإن التعرض الفعلي له أهمية كبيرة، ومن الصعب تقييم مستوى السمية دون معرفة التركيزات الفعلية.
المعروف أن الحطام البلاستيكي الأكبر حجماً يمكن أن يتفتت إلى مواد بلاستيكية نانوية، لكن لا يزال أمامنا الكثير لاكتشاف كيفية تعرض هذه الأجزاء لمزيد من التحلل. ويعمل الباحثون على اكتشاف وفهم المواد البلاستيكية النانوية عبر عديد من البيئات، حتى يتمكنوا من تطوير استراتيجيات فعالة لإدارة وتخفيف آثار هذه المواد على الناس والكوكب بوجه عام.
* أستاذ مساعد الهندسة المدنية والبيئية بجامعة «ويسكونسن - ماديسون»، مجلة «فاست كومباني»، خدمات «تريبيون ميديا».